|
Cholinchlorid in Wasser
|
|
Monte Carlo Simulation von Cholinchlorid in Wasser
Molekülstruktur und Merz-Kollmann Partialladungen des Cholin Kations wurden mit der Modellchemie PCM/HF/6-31G(d) mittels Gaussian09 in einer
PCM Wasserumgebung optimiert, anschliessend wurde ein RESP-Fit der Partialladungen durchgeführt (entsprechend Luzhkov et al., PCCP 2002, 4, 4640-4647).
Die Lennard-Jones Parameter für die MC-Simulation wurden von Morrow et al. übernommen (Morrow et al., Fluid Ph. Eq. 217 (2004) 97-104). Die MC-Simulation
wurde mit Ewald-Summation durchgeführt. In der Simulationsbox befanden sich unter Standardbedingungen 1024 SPC/E-Wasserteilchen, 12 Cholin Kationen und
12 Chlorid Anionen. Nach der Äquilibrierung umfasste die gesamte Simulation 160000 Simulationsschleifen, wobei von der Annahme ausgegangen werden kann,
dass eine MC-Simulationsschleife ca. 0.01 ps in der MD-Simulation betragen könnte.
|
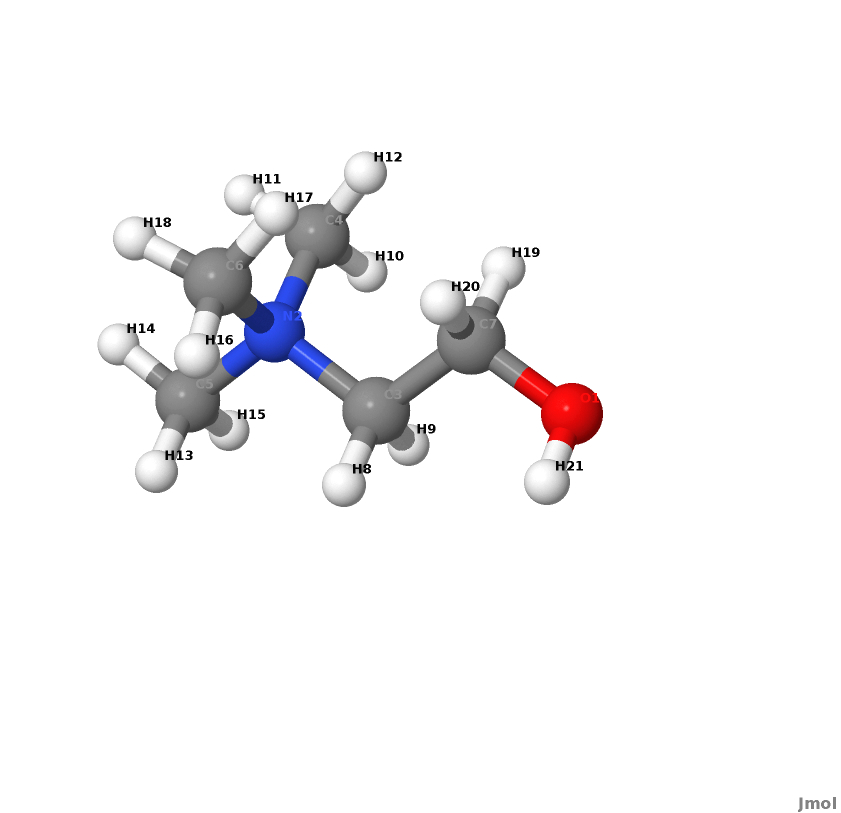
Nummerierung der Sites in einem Cholin Kation
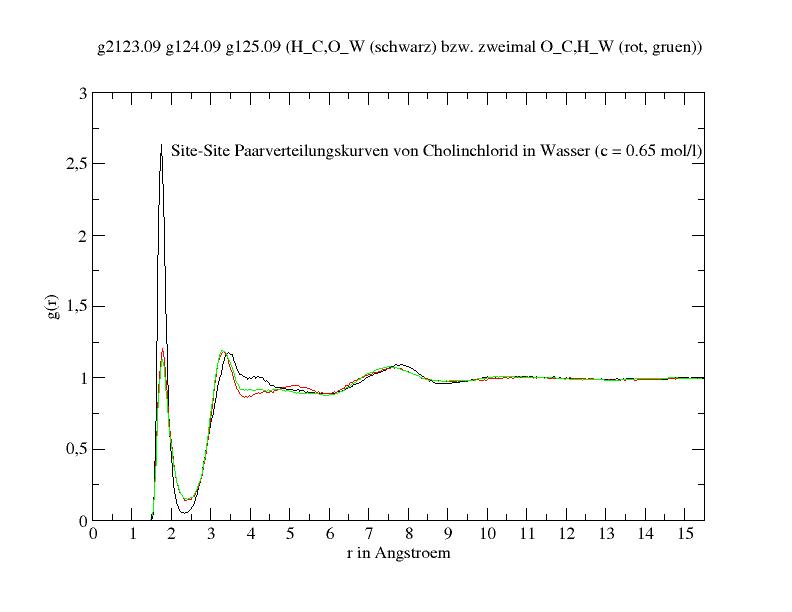
Site-Site Paarverteilungskurven
Der Abstand zwischen H-Site der Cholin-OH-Gruppe und O-Site des Wassers beträgt
genau wie der Abstand zwischen O-Site der Cholin-OH-Gruppe und H-Site des Wassers ca. 1.75 Angstroem.
Jedoch tritt ersteres bevorzugt auf.
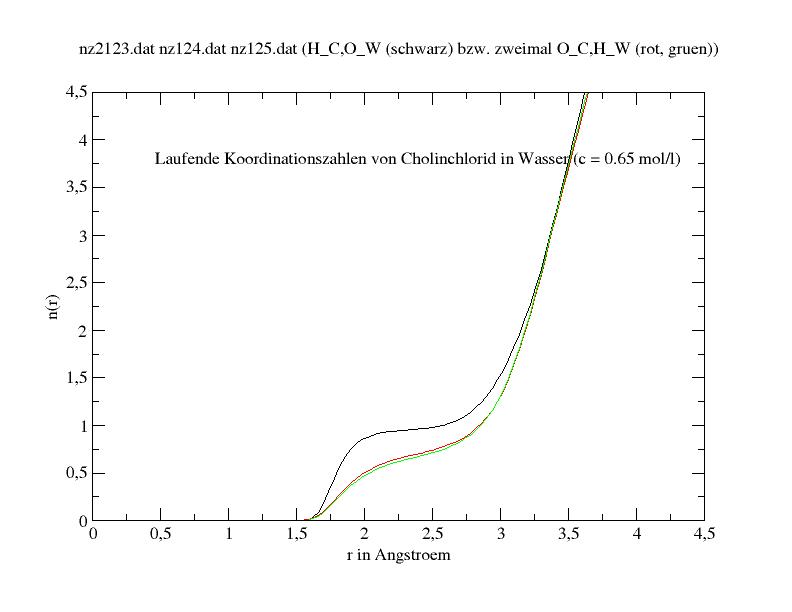
Laufende Koordinationszahlen der OH-Gruppe am Cholin
Die den obigen Site-Site Paarverteilungskurven entsprechenden laufenden Koordinationszahlen zeigen
dann auch zwischen 1.5 Angstroem und 2.5 Angstroem einerseits eine stabile Koordination zwischen dem O-Site von 1 Wassermolekül
und dem H-Site der Cholin-OH-Gruppe (schwarz, n(1.75) = 1) und andererseits eine lockere Koordination zwischen dem H-Site von Wasser und dem
O-Site von Cholin (rot, grün).
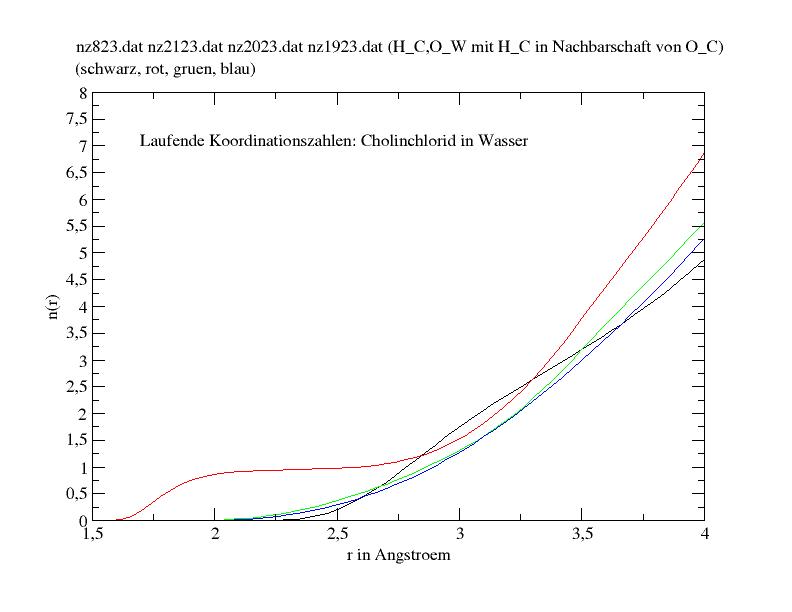
Laufende Koordinationszahlen der dem O-Site benachbarten H-Sites am Cholin
Betrachtet werden die H-Sites Nr. 8, 21, 20 und 19 am Cholin (siehe obige Nummerierungen der Sites in einem Cholin Kation)
relativ zum O-Site (Nr. 23) des Wassers. Die rote Kurve ist die obige schwarze Kurve (H-Site Nr. 21 gegen das O-Site des Wassers).
Des weiteren sieht man, dass ausser H-Site Nr. 21 nur H-Site Nr. 8 eine Koordination mit dem O-Site des Wassers eingeht,
wenn auch wesentlich lockerer (bei ca. 3.4 Angstroem mit n(r) = 3).
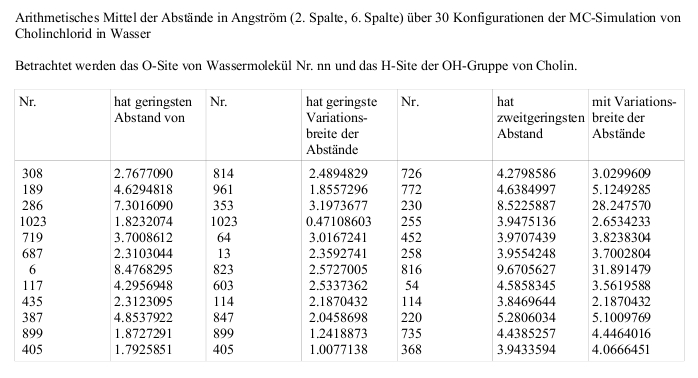
Mittlere Abstände zwischen dem O-Site eines Wassermoleküls und dem H-Site der OH-Gruppe von Cholin
Zu den ersten 4 Spalten:
Der Tabelle kann man entnehmen, dass das O-Site des Wassermoleküls Nr. 1023 einen mittleren Abstand von 1.823 Angström zum H-Site
der OH-Gruppe von Cholin einnimmt, bei einer geringen Variationsbreite aller seiner 30 gemessenen Abstände (gleichverteilt über den gesamten
Simulationszeitraum) von nur 0.471 Angström. Wassermolekül Nr. 1023 ist offenbar stark assoziiert.
Wassermolekl Nr. 308 ist nicht assoziiert. Wassermolekül Nr. 405 ist ebenfalls nicht assoziiert, da seine Abstands-Variationsbreite
1.008 Angström beträgt.
Zu den letzten 3 Spalten:
Im Falle von Wassermolekül Nr. 1023 ist Wassermolekül Nr. 255 das zweitnächstgelegene mit einem mittleren Abstand von 3.948 Angström
und einer Variationsbreite von 2.653 Angström. Es ist nicht assoziiert.
Insgesamt gesehen ist offenbar höchstens ein Wassermolekül mit einem Cholin Kation über einen längeren
Zeitraum assoziiert.
|
|
|
